2.1.1. Studi microbiologici
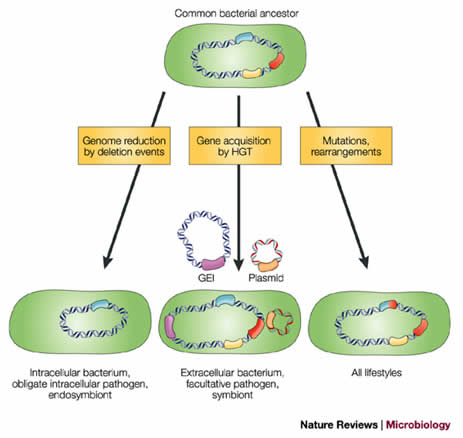
Gli studi microbiologici stanno riguardando come si creino e si sviluppino i batteri antibiotico-resistenti. L’occasione è a stata data da un’epidemia di salmonella resistente a ben 5 ceppi di antibiotici differenti nel 2000. In questa occasione i ricercatori hanno potuto individuare la presenza all’interno del batterio di un’isola genomica responsabile di trasmettere geneticamente la resistenza agli antibiotici. Quest’isola genomica è in grado di muoversi tra i batteri e si integra al nuovo batterio passando così le informazioni su come resistere agli antibiotici.
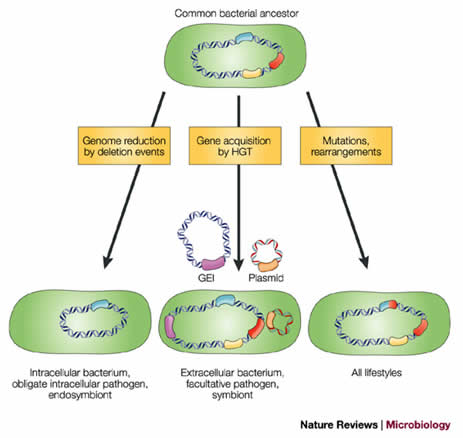

Meccanismo di integrazione dell’isola genomica in un batterio che consente al batterio di trasmettere ad altri i geni della resistenza
Crediti immagine: Nature
Ad oggi rimane ancora da capire nei dettagli come avvenga l’integrazione delle isole genomiche all’interno del genoma del batterio ricevente. Data la naturale capacità di adattarsi agli stress ambientali dei batteri, sarà molto difficile creare antibiotici che non provochino fenomeni di resistenza, tuttavia è possibile arrivare a produrne alcuni in grado di rallentare o inibire in parte lo sviluppo di una resistenza.